 글로벌 희귀의약품 시장 전망. /사진=윤선정 디자인기자
글로벌 희귀의약품 시장 전망. /사진=윤선정 디자인기자3일 업계에 따르면 최근 국내외 제약·바이오 기업들은 FDA의 ODD(희귀의약품 지정) 제도를 적극 활용해 희귀의약품 개발 경쟁에 뛰어들고 있다. ODD는 해당 질환 환자 수가 적고(통상 10만명 미만) 미충족 의료수요가 높은 치료제에 대한 인증으로, 제약사의 희귀의약품 개발 유인을 높이고자 마련된 제도다. 실제 ODD를 받은 기업은 R&D(연구·개발) 비용 절반에 대한 세금 감면·시판 후 7년간 독점권 부여 등 혜택이 제공된다. 인허가 속도를 높이는 일종의 패스트트랙으로 NDA(품목허가승인신청)와 직접적 관련은 없다.
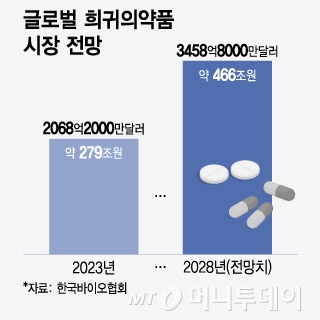
희귀의약품은 개발 난도가 높지만 고마진이 기대되는 '니치버스터'로 불린다. 환자 수가 적은 비주류 영역이다 보니 선점효과도 비교적 크다는 게 업계 입장이다. 실제 성장세도 가파르다. 한국바이오협회에 따르면 지난해 전 세계 희귀의약품 시장 규모는 2068억2000만달러(약 279조원)로, 2028년에는 3458억8000만달러(약 466조원)까지 커질 전망이다. 국내에서도 희귀의약품에 대한 관심은 높아지고 있지만 정작 희귀의약품으로 지정된 제품 수는 현저히 적다. 산업연구원에 따르면 2012~2021년 기준 희귀의약품 지정 수는 △미국 3241건 △EU 1279건 △일본 244건 △한국 173건으로 조사됐다.
한 국내 바이오 업계 관계자는 "일본의 경우 허가제와 신고제 두 가지로 의약품 제도가 나뉘어서 운영되기 때문에 시판까지의 허들은 한국과 비교했을 때 상당히 낮은 편"이라며 "임상 1상부터 기본 3억~4억원이 드는데, 희귀의약품의 경우 개발 비용 회수 가능성이 매우 낮다는 인식 탓에 기업 입장에선 개발 유인이 적은 게 사실"이라고 말했다. 또 다른 관계자는 "상대적으로 희귀의약품 개발 성공 사례가 부족한 국내 기업은 이미 선두주자로 있는 글로벌 대형 제약사와 협업을 통해 성과를 내는 경험도 중요하다고 본다"며 "관계부처가 나서서 파트너사 연계나 투자 관련 컨설팅 등 지원에 적극적으로 나서야 한다"고 전했다.
