엔케이맥스는 30일(미국시간) 미국임상종양학회(ASCO)에서 자회사 엔케이젠바이오텍이 진행중인 불응성 고형암(육종암) 임상 1상에 대한 포스터 2건을 공개했다. 공개된 포스터는 슈퍼NK(SNK01) 단독투여군, 슈퍼NK+바벤시오(성분명: 아벨루맙) 병용투여군에 대한 임상 내용이다.
슈퍼NK와 바벤시오 병용투여군 포스터에는 코호트4에 속하는 총 17명의 육종암 환자에 대한 중간 결과가 공개됐다. 다만 두명에 대한 데이터는 아직 도출해 내지 못해 이번 포스터에는 추가되지 못했다. 병용투여 결과 표적병변에서 완전관해 1명, 종양이 30%이상 줄어든 부분관해(PR)환자가 1명, 종양이 더 이상 자라지 않는 SD환자가 8명 관찰됐다. CR이 확인된 환자의 경우 비표적병변에 종양이 남아있어 미국 식품의약국(FDA)의 기준에 따라 PR로 초록에 표시됐다.
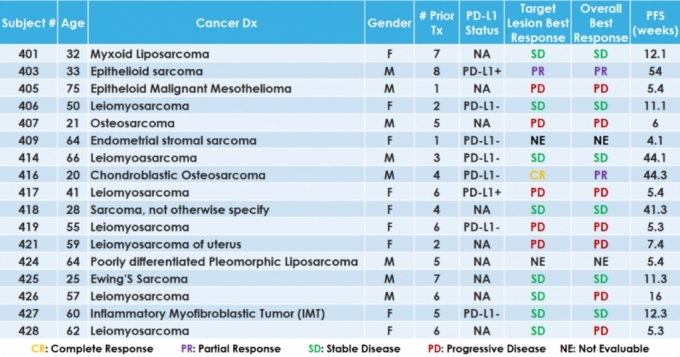 미국임상종양학회(ASCO)에 채택된 슈퍼NK+바벤시오(성분명: 아벨루맙) 병용투여군 결과 포스터
미국임상종양학회(ASCO)에 채택된 슈퍼NK+바벤시오(성분명: 아벨루맙) 병용투여군 결과 포스터현재 글로벌 제약사들이 육종암 치료제 개발에 도전하고 있지만 아직 뚜렷한 두각을 나타내지 못하고 있는 상황이다. 아스트라제네카의 올라파립(Olaparib) 또는 세디라닙(cediranib)과 병용투여한 더발루맙(Durvalumab)은 평활근육종을 대상으로 임상2상을 진행했으나 치료반응률(ORR)이 0%에 그쳤다. 항암치료 이후 종양의 크기 변화가 없는 안정병변(SD)은 33%에 머문 반면 항암치료 진행에도 종양의 크기가 커지는 진행병변(PD)는 67%로 나타났다.
머크는 재발 및 진행성 골육종 환자를 대상으로 바벤시오 약물 단독투여 임상2상을 진행했으나 임상 16주차에 모든 대상환자(17명)들의 증세가 진행성으로 악화되며 바벤시오 약물 단독으로는 치료효과를 보지 못했다.
이 시각 인기 뉴스
그러나 엔케이맥스의 미국 불응성 고형암(육종암) 임상 1상에서 슈퍼NK와 바벤시오를 병용투여한 결과 표적병변 CR상태가 확인됐다. 포스터에 따르면 치료반응률(ORR) 11.7%이며 중앙값 무진행생존기간(Median PFS) 11.14주로 나타났다. 특히 4명의 환자가 41주 이상의 무진행생존을 보였다. 아울러 중앙값 전체 생존기간(Median OS) 24.9주로 확인됐다. 이에 슈퍼NK와 면역관문억제제의 병용요법이 육종암 환자의 새로운 치료방법으로 제시될 것으로 기대된다.
엔케이맥스는 임상과 별개로 동정적사용승인을 받아 진행했던 말기 육종암 환자에게서도 암이 완전히 사라지는 CR상태를 확인했다. 지난 4월 동정적사용승인으로 2년 6개월간 슈퍼NK와 키트루다(성분명: 펨브롤리주맙)를 병용투여한 결과 CR을 확인했다고 회사 측은 전했다.
이 환자의 경우 28개월간 30회 이상 투여를 진행했으며, 치료 이전에는 복부를 포함하여 대부분의 장기에 암이 전이된 상태였던 것으로 알려졌다. 해당 환자는 2019년 엔케이맥스의 불응성 고형암 임상 1상 코호트1에 등록돼 일주일 간격으로 슈퍼NK를 5회 투여 받은 뒤 종양의 진행이 멈춰 임상과 별개로 미국 FDA의 동정적 사용 승인을 받아 슈퍼NK와 키트루다를 병용투여 받았다. 이후 28개월동안 총 30회 슈퍼NK와 키트루다를 병용투여 받았고, 그 결과 온몸에 전이됐던 암이 완전히 사라진 CR 상태가 확인됐다.
회사 관계자는 "온 몸에 암이 전이된 육종암 말기 환자들은 대부분 기대수명이 6개월 이내이다"며 "엔케이맥스는 이러한 시한부 환자들을 대상으로 임상을 진행하고 있기 때문에 말기 육종암 환자를 대상으로 암의 증식을 억제하는 것만으로도 의학적으로 의미 있는 결과를 도출한 것으로 보인다"고 말했다.
