 /사진=정춘숙 더불어민주당 의원실
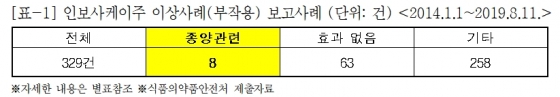
/사진=정춘숙 더불어민주당 의원실4일 국회 보건복지위원회 소속 정춘숙 더불어민주당 의원이 식약처로부터 제출받은 '인보사 이상사례(부작용) 보고사례' 자료에 따르면 지난 2014년 1월1일부터 올해 8월11일까지 부작용 329건이 보고됐다.
앞서 인보사는 지난 3월 제품 주성분이 뒤바뀐 것이 밝혀져 판매 중지되고, 지난 7월 품목허가가 취소됐다. 이 과정에서 바뀐 성분이 종양 유발 가능성이 있는 신장유래세포(293유래세포)인 것으로 드러나면서 논란이 일었다. 코오롱생명과학 측은 방사선 조사 과정을 통해 종양 유발 가능성을 차단했다고 주장하고 있다.
정 의원은 "역학조사를 실시하지 않고 있느냐 재차 확인하자 그제서야 식약처는 재검증을 지시한 것으로 확인했다"며 "위암 같은 종양 관련 보고가 접수됐음에도 식약처사 역학조사 조차하지 않다는 것은 문제가 있다"고 지적했다.
이어 "대부분의 전문가들은 인보사 관련 안전성 우려가 크지 않다고 하지만 종양 유발 가능성 등을 이유로 현재 환자 장기추적조사 등이 이뤄지고 있다"며 "식약처의 더욱 적극적인 환자안전관리 대책이 필요하다"고 말했다.
