셀트리온은 지난달 29일(유럽 현지시간) 자가면역질환 치료용 항체 바이오시밀러 '램시마SC(피하주사 제형, 성분명 인플릭시맙)'에 대한 허가 서류를 유럽의약품청(EMA)에 공식 접수했다고 3일 밝혔다.
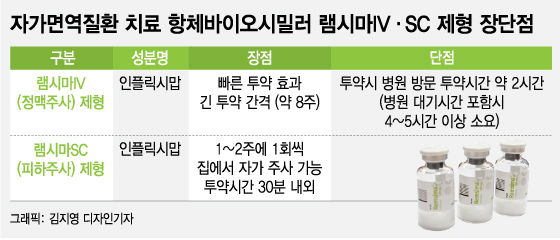
기존 램시마는 IV제형으로 빠른 투약효과는 있으나 2시간 이상 소요되는 정맥 투여를 위해 병원에 반드시 방문해야 했다. 하지만 SC제형은 환자가 집에서 의약품을 보관하다가 사용 주기에 맞춰 피하에 자가 투여하면 된다. 이때 투여시간은 30분 내외다.
특히 램시마SC는 자가면역질환 치료제 시장 중 염증성 장질환(IBD) 분야에서 더욱 큰 성장이 기대된다.
최근 유럽 크론병 및 대장염학회(ECCO)에서 발표된 크론병 환자별 맞춤 치료 임상(PANTS Study) 결과에 따르면, IBD 환자군에서 램시마가 휴미라 대비 높은 관해율·반응율을 보였다. 그러나 램시마는 정맥주사 제형이라는 한계점 때문에 피하주사 제형인 휴미라와의 경쟁에서 밀려왔다.
이 시각 인기 뉴스
셀트리온은 램시마 SC가 출시될 경우 휴미라가 독점해왔던 IBD 시장 판도가 크게 바뀔 것으로 전망했다.
셀트리온 관계자는 "염증성 장질환 분야에서 인플릭시맙의 효과가 더욱 뛰어나지만 편의성 등의 측면에서 아달리무맙에게 밀려왔다"며 "램시마SC 제형이 출시되면 휴미라 독점 구조를 깨드릴 수 있을 것"이라고 기대했다.
이어 "전세계 자가면역질환 치료제 시장에서 피하주사 제형의 매출은 약 30조원을 차지할 만큼 큰 시장"이라며 "셀트리온은 유럽 시장에서 이미 52%의 점유율을 기록한 정맥주사 제형의 램시마와 램시마 SC 등을 통해 전세계 자가면역질환 치료제 시장을 선도해 나갈 계획"이라고 강조했다.
