22일 업계에 따르면 20일(현지시간) 미국 식품의약국(FDA)은 삼성바이오에피스 '오퓨비즈'와 인도 바이오콘 '예사필리' 등 2종의 아일리아 바이오시밀러에 대한 품목 허가를 승인했다. 미국에서 허가 받은 첫 아일리아 시밀러인 동시에 나란히 오리지널과 상호 교환 가능한 인터체인저블 시밀러 지위도 획득했다.
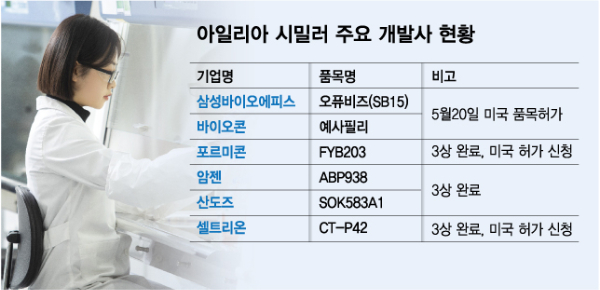
아일리아는 미국 내 물질 특허가 지난해 6월 만료됨에 따라 삼성바이오에피스를 비롯한 다수 개발사들이 바이오 시밀러 허가에 도전해 왔다. 실제로 삼성바이오에피스와 바이오콘 외 포르미콘, 암젠, 알보텍, 산도즈, 셀트리온 등이 3상을 완료해 허가 절차에 돌입한 상태다.
특히 삼성바이오에피스는 이번 허가로 미국에서 아일리아와 루센티스 시밀러를 모두 허가받은 유일한 기업에 이름을 올리게 됐다. 이미 앞서 허가받은 루센티스를 현지 파트너사인 바이오젠이 판매 중인 만큼 발 빠른 시장 진입 기반이 다져졌다.
오리지널사 리제네론, 고용량 출시로 대응…진행 중인 특허 소송도 출시 시기 변수로다만 현지 시장 공략을 위한 허들도 남아있다. 리제네론이 지난해 하반기 아일리아 고용량 품목(아일리아HD)을 출시하며 점유율 방어에 나선 상태다. 용량을 8㎎으로 늘려 최대 12~16주 간격까지 투약 주기를 확대한 것이 특징이다. 안구에 직접 주사하는 주사제 특성상 1~2달 새 처방해야 하는 기존 아일리아 대비 환자 순응도가 높을 수밖에 없다.
이 시각 인기 뉴스
고용량 제품의 시장성은 지난해 특허 만료로 바이오시밀러가 대거 시장에 쏟아진 애브비 자가면역질환 치료제 '휴미라' 사례가 잘 보여줬다. 지난해 1월 암젠 '암제비타'가 첫 시밀러로 허가 받았지만, 저용량 품목 한계상 후속 고용량 품목들에 점유율을 역전당했다. 현재 미국 휴미라 시장 내 고용량 제품의 점유율은 85%에 이른다.
아일리아의 경우 고용량 제품 출시가 최근에 이뤄져 아직 반수 이상의 점유율을 기록하고 있진 않지만, 역전은 시간 문제라는 평가가 지배적이다. 이를 잘 알고 있는 시밀러 개발사들 역시 아일리아 고용량 품목 연구를 진행 중이지만, 아직 허가 신청 단계에 이른 품목은 없는 것으로 알려졌다.
리제네론이 삼성바이오에피스를 비롯한 다수 기업을 대상으로 제기한 특허 소송도 변수다. 시밀러 개발사를 상대로 한 오리지널 개발사의 소송전은 시장 진입 지연을 위해 일반적으로 사용되는 전략이다. 이 경우 시밀러 개발사들은 일정 위약금이나 로열티를 주고 출시 시기를 확정하는 경우가 잦다.
이른 출시가 곧 경쟁력인 시밀러 시장 특성상 특허 합의를 통해 출시 시기를 조율하고, 일정 확정을 통해 효율적인 마케팅 전략을 수립하는 것이 중요하기 때문이다. 삼성바이오에피스 역시 스텔라라 시밀러에 대해 지난해 11월 오리지널 개발사인 존슨앤존슨(J&J)과의 특허 합의를 통해 내년 2월 제품을 출시할 수 있다.
현재 리제네론이 삼성바이오에피스에 제기한 소송의 세부 종류와 결과 관련 일정에 대해 공개된 것은 없는 상태다. 다만 아직 삼성바이오페이스가 오퓨비즈 출시 일정 등에 대해 세부적으로 공개하지 않는 배경 역시 해당 변수의 우선 해소에 무게를 둔 것으로 풀이된다.
삼성바이오에피스 관계자는 "미국 파트너사의 경우 앞서 바이오젠과 루센티스 판매를 협업하는 단계에서 이미 아일리아 시밀러도 함께 하기로 논의를 마쳤지만, 현지 출시 일정 등에 대해 현재로서 언급할 수 있는 내용은 없는 상태다"고 말했다.
