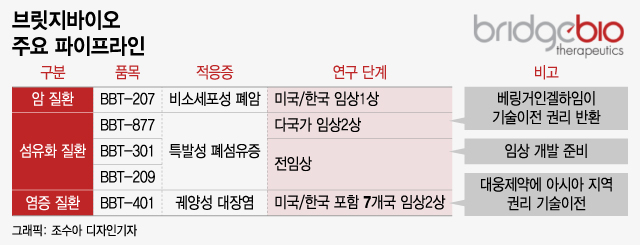
브릿지바이오는 주요 파이프라인인 비소세포성 폐암 치료제 후보물질인 'BBT-207'과 특발성 폐섬유증 치료제 파이프라인 'BBT-877'의 임상시험을 순조롭게 진행하고 있다고 28일 밝혔다.
하지만 상장 뒤 1년이 채 지나지 않은 2020년 11월 베링거인겔하임은 BBT-877의 모든 권리를 반환했다. 브릿지바이오는 BBT-877와 궤양성 대장염 치료제 'BBT-401'의 기술이전 계약으로 2020년 827억원의 매출을 올릴 것으로 추정했지만, 현실은 63억원에 불과했다.
브릿지바이오는 적자가 지속되는 상황에서 일부 파이프라인의 연구를 중단하기도 했다. 폐암 치료제로 개발하던 'BBT-176'의 한국 및 미국 임상 1/2상 시험을 지난 9월 자진 취하했다. 자진 취하 사유로 'BBT-207'에 집중하기 위해서라고 설명했다. 또 건국대학교 산학협력단으로부터 도입한 안저질환 치료제 후보물질 'BBT-212'의 공동연구 계약도 지난 9월 해지했다. 앞서 지난 2월엔 궤양성 대장염 치료제 BBT-401의 임상 2a상에서 유효성을 확인하지 못했다고 발표했다.
브릿지바이오는 서둘러 상업화 성과를 확보해야 한다. 법인세차감전계속사업손실(법차손)에 따른 관리종목 지정 우려에 노출될 수 있기 때문이다. 브릿지바이오는 2019년 12월 기술특례로 상장해 법인세차감전계속사업손실 발생에 따른 관리종목 지정이 2022년 말까지 유예됐다. 올해부터 자기자본 50% 이상의 법인세차감전계속사업손실이 3년간 2회 이상 발생할 경우 관리종목으로 지정될 수 있다.
이 시각 인기 뉴스
브릿지바이오는 BBT-207과 BBT-877에 집중해 기술이전 성과를 확보하겠단 목표다.
BBT-207은 폐암 치료제 '타그리소'(Tagrisso)의 내성 환자를 위한 비소세포성 폐암 치료제 후보물질이다. 올해 4월 미국 식품의약국(FDA), 8월 한국 식품의약품안전처(식약처)로부터 임상 시험계획(IND)을 승인받고 임상 1상을 진행하고 있다.
BBT-877은 베링거인겔하임이 기술이전 권리를 반환했지만, 2022년 7월 미국 FDA로부터 임상 2상 IND를 승인받았다. 현재 미국을 포함한 여러 국가에서 임상 2상을 진행하고 있다. 다시 기술이전을 추진할 계획이다.
브릿지바이오 관계자는 "BBT-207은 임상 단계에 진입한 뒤 순조롭게 환자 투약을 진행하고 있고, BBT-877은 다국가 임상 2상에 진입했다"며 "BBT-207과 BBT-877을 앞세워 다양한 글로벌 협업 기회를 살피고 있다"고 말했다. 또 "바이오에 대한 주식시장 평가가 좋지 않지만 기술이전 등 상업화 성과를 신속하게 확보하기 위해 노력하겠다"며 "이외에 임상 조직을 기반으로 다른 바이오와 협업해서 사업화를 꾀하는 신사업도 추진하고 있다"고 말했다.
