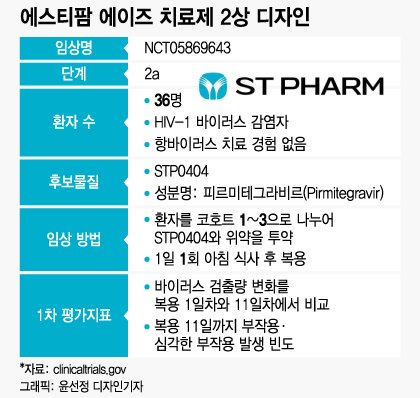
26일 업계에 따르면, 에스티팜의 STP0404(성분명: 피르미테그라비르) 임상 2a상 정보가 최근 미국 국립보건원 임상 정보 사이트(clinicaltrials.gov)에 게재됐다. STP0404는 후천성 면역 결핍증(AIDS·에이즈)을 유발하는 HIV-1 바이러스를 치료하는 약으로 개발되고 있다.
STP0404 저·중·고 용량과 플라시보(위약)를 세 개의 환자 집단(코호트 1~3)에서 각각 투약한다. 누가 위약을 먹었는지 환자도, 의사도 알 수 없는 이중맹검 시험이다. STP0404는 캡슐 형태의 약으로 1일 1회, 아침 식사 후 복용한다.
첫 환자 투약은 다음 달 예정돼 있다. 임상 시험 1차 종료일은 2024년 1월 10일이다.
STP0404는 알로스테릭 인테그라제 효소 저해제(Allosteric Integrase Inhibitor·ALLINI)다. 이 기전으로 인체 대상 임상 시험에 들어간 후보물질은 STP0404가 유일하다. 계열 내 최초 신약(First-in-class)이 될 가능성이 있다. 앞서 글로벌 빅파마 길리어드사이언스가 같은 기전의 후보물질 'GS-9822'를 개발했으나 안전성 이슈로 전임상 단계에서 연구를 중단한 바 있다.
이 시각 인기 뉴스
에이즈는 장기간 관리해야 하는 병이라 약을 평생 먹어야 한다. 내성 문제가 발생하기 때문에 환자가 다른 기전의 여러 약물을 돌려막기식으로 복용하기도 한다. STP0404은 새로운 기전의 약물이라 내성 문제에서도 자유롭다는 게 회사 측 설명이다.
7월 말 열리는 제7회 국제 레토르바이러스 학회도 주목해야 한다. 이 자리에서 STP0404 작동 원리(메카니즘)를 밝힌 논문이 발표되기 때문이다. 미국 콜로라도 대학과 하버드 대학 그리고 영국 임페리얼 대학 등에서 두 건의 논문을 발표한다.
또한 학회에서는 김경진 에스티팜 대표가 STP0404 개발 과정을 메인 세션에서 구두로 발표한다. 전임상과 임상 1상 결과도 포스터 형식으로 공개될 예정이다. 지난해 에스티팜은 65명의 건강한 성인 남성을 대상으로 진행된 임상 1상에서 약물의 안전성을 확인했다고 밝혔다.
에스티팜 관계자는 "신약을 라이선스 아웃할 때 메커니즘이 굉장히 중요하다"며 "글로벌 제약사는 어떤 원리에서 약의 효과와 안전성이 나왔는지 명확하게 규명되길 원한다"고 설명했다.
이어 "이번 학회에서 STP0404의 결정 구조체는 무엇이고, 이론적으로 어떻게 작동하는지 입증하는 논문이 발표되기 때문에 굉장히 의미가 크다"고 했다.
그러면서 "임상 1상에서 안전한 약물이라고 확인됐으니 2상에서 효능만 제대로 나오면 단독 사용으로도 에이즈 완치를 노릴 수 있는 원리의 약물이다. 병용 치료제로도 개발할 수 있다"고 말했다.
