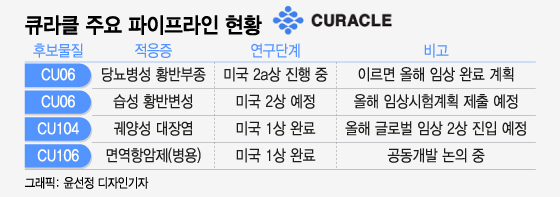
큐라클은 당뇨병성 황반부종 치료제 미국 임상 2a상을 순조롭게 진행하고 있다고 12일 밝혔다. 현지에서 임상 기관을 확대하며 환자 모집 속도가 빨라지고 있단 설명이다.
큐라클은 당뇨병성 황반부종 환자 60명을 대상으로 하는 CU06 임상 2a상 결과를 확인하는 대로 후속 임상에 바로 진입할 계획이다. 망막질환은 비교적 약물 투여 기간이 길지 않아 다른 신약보다 상대적으로 임상 시험 속도가 빠른 편이다. 당뇨병성 황반부종 치료제는 아직 허가 받은 경구용(먹는) 치료제가 없어 큐라클이 상업화에 성공할 경우 의료 현장의 수요는 충분할 것으로 예상된다. 전 세계 시장 규모는 2025년 32억달러(약 4조2000억원)로 성장할 것으로 전망된다.
큐라클이 집중하고 있는 궤양성 대장염 치료제 CU104에 대한 관련 업계의 관심도 적지 않다. 글로벌 제약사의 연구 경쟁이 치열한 영역이라 큐라클의 도전이 더 의미가 있다. 최근 CU104 임상 개발 경쟁력을 높이기 위해 서울대학교 약학대학 임상약학 연구실과 협업을 약속했다. 서울 약대의 여러 전문가가 CU104 임상 연구에 힘을 보탤 예정이다.
큐라클은 앞서 CU104 미국 임상 1상을 완료한 데 이어 올해 미국 FDA(식품의약국)에 임상 2상 시험 계획(IND)을 제출할 예정이다. 시장성이 뛰어난 파이프라인인 만큼 미국 임상 2상 시험 계획이 승인될 경우 글로벌 시장의 주목도가 높아질 것으로 기대된다.
이 시각 인기 뉴스
큐라클의 병용 면역항암제 파이프라인 CU106은 미국 임상 1상 완료 뒤 공동 개발 파트너를 찾고 있다. 비교적 임상 개발 난이도가 높은 항암제 파이프라인인 만큼 공동으로 임상 연구를 수행할 수 있는 전략적 파트너를 구하겠단 전략이다. 여러 기업이 관심을 보이고 있단 후문이다.
큐라클 관계자는 "CU06 미국 임상 2상은 첫 환자 투약 뒤 여러 기관에서 환자를 순조롭게 모집하며 문제없이 진행되고 있다"며 "CU06 임상을 진행하는 한편 궤양성 대장염 치료제 CU104의 임상 연구에서 성과를 내기 위해 역량을 집중하고 있다"고 말했다.
또 "특히 CU104는 글로벌 선두권 제약 기업들이 치열하게 연구하는 궤양성 대장염 치료제 파이프라인으로 큐라클이 혁신신약으로 제대로 승부를 걸어볼 생각"이라며 "미국 FDA 임상 2상 시험 계획 신청 뒤 상황에 따라 정부 과제로 개발하는 방안 등을 검토하고 있다"고 말했다.
