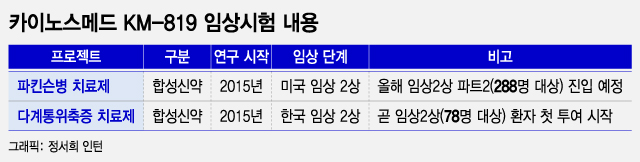
카이노스메드는 다계통 위축증 치료제를 개발하기 위한 국내 임상 2상의 첫 환자 투약이 이르면 이달 가능할 것으로 예상된다고 14일 밝혔다.
카이노스메드는 다계통 위축증 환자 78명을 대상으로 국내에서 임상 2상을 시작했다. 현재 환자 모집 단계로 이르면 이달, 늦어도 내달 첫 환자 투약이 이뤄질 예정이다. 올해 3분기엔 모든 환자에 대한 투약이 가능할 것으로 보인다. 이후 9개월이 지나면 중간 결과가 나온다. 임상 과정이 순조로울 경우 내년 상반기엔 중간 결과를 확인할 수 있다. 매우 드문 희귀 질환인 만큼 임상 2상 결과에 따라 조건부 허가도 기대할 수 있다.
파킨슨병 치료제 미국 임상 2상도 예정대로 절차가 진행되고 있다. 이 임상은 3단계로 구분하는데, 첫 번째 단계인 18명 대상 파트1 A를 성공적으로 마쳤다. 이를 통해 안전성을 확인했다. 다음 단계인 24명 대상 파트1 B에 곧 진입할 예정이다.
임상 2상의 핵심인 파킨슨병 환자 288명을 대상으로 진행하는 세 번째 단계인 파트2는 연내 진입할 계획이다. 이후 약 2년간 경과를 지켜보는 일정이다.
이 시각 인기 뉴스
카이노스메드는 파킨슨병 임상 2상을 완료한 뒤 기술이전에 나설 계획이다. 파킨슨병 치료제 시장은 2026년 약 88억달러(약 11조5000억원) 규모로 성장할 것으로 전망된다. 전 세계적인 인구 고령화 추세에 따라 환자 수가 갈수록 늘어날 가능성이 크다. 파킨슨병 치료제 임상 2상 결과에 따라 카이노스메드의 위상이 급격하게 달라질 수 있다.
이재문 카이노스메드 사장은 "KM-819의 다계통 위축증 치료제 개발을 위한 국내 임상 2상의 중간 결과가 내년에 나오면 파킨슨병 치료제 미국 임상 2상에 대한 기대감도 커질 것"이라며 "의료적으로 미충족 수요가 높은 질환에 대한 혁신신약인 만큼 임상 2상 결과가 긍정적으로 나올 경우 글로벌 시장에 미치는 파급력이 매우 클 것으로 기대하고 있다"고 말했다.
