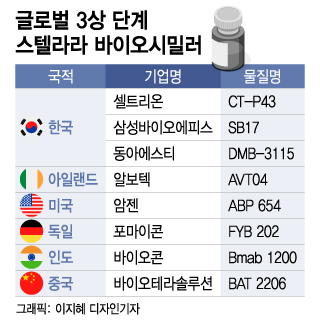
7일 관련업계에 따르면 알보텍은 지난 1월과 2월 각각 미국 식품의약국(FDA)과 유럽의약품청(EMA)에 스텔라라 바이오시밀러 'AVT04'의 품목허가 신청을 승인받았다. 두 지역 모두 연내 승인 여부가 결정될 전망이다.
미국 얀센이 개발한 스텔라라는 판상 건선을 비롯해 건선성 관절염, 크론병, 궤양성 대장염 등 다양한 염증성 질환에 사용되는 치료제다. 지난 2021년 매출액이 91억3400만달러(약 11조8700억원)에 이르는 글로벌 블록버스터 품목이다. 하지만 오는 9월 미국, 내년 7월 유럽에서 물질특허 만료를 앞두고 있다.
다만 가장 먼저 신청에 나선 알보텍의 허가 여부가 연말쯤 도출될 것으로 보이는 만큼, 당장 올해 스텔라라 시밀러의 시장 출시는 불가능한 상황이다. 때문에 경쟁사 대부분 올해 허가 신청에 나서 내년 시장 출시를 목표로 하고 있다.
국내사 중에선 동아에스티가 'DMB-3115'의 상반기 내 유럽 및 미국 허가 신청 계획을 밝힌 상태다. 동아에스티는 지난 2021년 미국을 비롯한 9개국에서 605명의 환자를 대상으로 한 DBM-3115 글로벌 3상에 돌입, 지난 1월 동등성과 안전성을 확인한 톱라인(핵심) 결과를 확인했다.
이 시각 인기 뉴스
미국·유럽 내 바이오의약품 허가 경험이 없다는 게 약점으로 꼽히지만, 유럽 임상에서 경쟁사(12주) 대비 이른 8주 만에 효능을 입증해 자신감은 충분한 상태다. 또 글로벌 90여개국 판매망과 10종 이상의 바이오시밀러 상용화 경험을 보유한 인타스와 파트너십을 통해 상용화 대비도 마쳤다.
셀트리온과 삼성바이오에피스는 전략상 세부 허가 신청 시점을 밝히지 않았다. 다만 스텔라라 허가만료 시기와 동아에스티 등 경쟁사 신청 및 시장 진입 시점 등을 고려하면 유사한 시기에 허가 신청에 나설 것이 유력하다.
내년 출시를 목표로 'CT-P43'을 개발 중인 셀트리온의 강점은 직판체제를 기반으로 한 가격 경쟁력이 될 것으로 보인다. 현지 유통 파트너를 통해 시장에 진입하는 경쟁사와 달리 유럽에서 직판체제 구축을 완료한 데 이어 올해 미국에서 직판체제 전환에 속도를 내고 있다. 유통 구조 단순화를 통한 원가 절감으로 시밀러 핵심 경쟁력으로 꼽히는 가격 책정에 유리하게 작용할 전망이다. 경영 복귀를 선언한 서정진 명예회장의 존재 역시 속도감을 더해줄 요소로 꼽힌다.
삼성바이오에피스는 일찌감치 글로벌 바이오시밀러 시장에 진출해 이미 5개 품목을 상용화 한 경험과 3개 자가면역질환 치료제 파이프라인을 기반으로 한 시너지 효과가 강점이다. '유럽-바이오젠, 미국 및 기타지역-오가논'과 지속된 유통 파트너십 역시 신규 품목의 시장 안착에 든든한 배경으로 작용할 전망이다.
