12일 관련 업계에 따르면 휴온스 (34,350원 ▲50 +0.15%)는 최근 안구건조증 치료제 후보물질 'HU007'에 대해 식품의약품안전처로부터 국내 임상 3상을 승인받았다.
HU007은 항염효과를 내는 사이클로스포린과 눈물막 보호 효과를 내는 트레할로스를 복합한 점안제 후보물질이다. 회사는 안구건조증 환자 328명을 대상으로 엘러간의 레스타시스와 유효성, 안전성을 비교할 계획이다.
HLB테라퓨틱스는 무려 네 번째 임상 3상에 도전한다. 회사는 미국 식품의약국(FDA)에 안구건조증 치료제 후보물질 'RGN-259'의 미국 임상 3상 설계에 대한 사전 논의를 신청했다.
안구건조증은 눈물을 분비하는 눈물샘의 이상으로 생기는 질환이다. 눈이 뻑뻑하거나 모래알이 들어간 것 같은 이물감이 대표적인 증상이다.
이 시각 인기 뉴스
라식수술의 부작용으로도 꼽힌다. FDA는 10년에 걸쳐 라식수술의 부작용 합병증 등에 대한 경고 지침을 준비중인데 여기에 안구건조증이 생길 수 있다는 내용이 담길 것으로 점쳐진다. 라식수술은 미국에서만 매년 50만명 이상이 받는다.
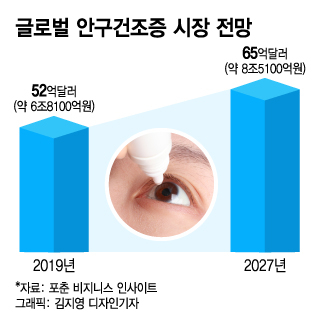
스마트폰 사용이 늘고 미세먼지 같은 환경적인 요인으로 안구건조증 환자는 증가할 것으로 전망된다. 시장조사기관 포춘 비지니스 인사이트에 따르면 2019년 59억달러(약 6조8100억원)에서 2027년 65억달러(약 8조5100억원)까지 늘어날 것으로 추산된다. 연 평균 성장률은 4.7%다.
빠른 성장이 예고되지만 시장은 과점 구조다. 안구건조증 치료제 시장은 크게 애브비의 레스타시스, 노바티스의 자이드라가 양분하고 있다. 두 품목만 FDA의 승인을 받았다. 일본 제약사 산텐도 디쿠아스를 개발했지만 FDA의 문턱을 넘지못해 주로 일본, 한국에서만 판매된다.
이 같은 구조가 공고해진 것은 안구건조증 치료제는 제약사가 개발하기 쉬운 품목이 아니기 때문이다. 임상시험 과정에서 환자가 느끼는 주관적인 증상 개선과 의사가 판단하는 징후 지표를 모두 충족해야 한다. 애브비의 레스타시스는 2014년 특허가 만료됐음에도 올해 2월 첫 복제약(퍼스트 제네릭)이 FDA의 승인을 받았다.
국내 업체가 여러 번의 임상시험을 거쳐 개발에 성공할 경우 블록버스터 약물로 자리잡을 수 있다. 동시에 여러번의 임상에서 유효성을 증명하지 못한다면 약물의 경쟁력이 낮을 가능성도 있다. 한 업계 관계자는 "과점 시장에 기존 치료제보다 더 효과가 좋은 제품으로 진입하면 우위를 점할 가능성이 클 것"이라면서 "다만 하나의 적응증에 대해 임상시험을 여러 번 진행하고 매번 유의성을 확보하지 못한다면 약물의 경쟁력을 따져봐야 하지 않겠나"라고 했다.
