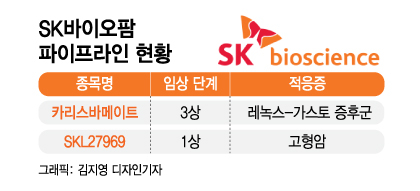
14일 제약·바이오업계에 따르면 SK바이오팜은 최근 식품의약품안전처로부터 '카리스바메이트'의 국내 임상 3상을 허가받았다.
카리스바메이트는 레녹스-가스토 증후군을 치료하는 신약이다. 레녹스-가스토 증후군은 여러 종류의 발작 증상이 나타나는 희귀 난치성 소아 뇌전증으로 발달 및 행동 장애를 동반한다. 현재는 완치법이 없고 치료 예후도 좋지 않아 환아의 약 85%가 성인이 된 후에도 발작을 지속 경험한다. 세계적으로 약 100만명의 환자가 있는 것으로 추정된다.
한 업계 관계자는 "국내에서도 임상 3상이 시작돼 카리스바메이트 임상 종료 후 허가시 국내외에서 비슷한 시기에 출시될 것으로 보인다"고 말했다.
카리스바메이트 임상 3상과 함께 항암 신약 개발도 속도를 낸다. 미국에서 임상 1상이 진행중인 항암신약 'SKL27969'는 국내에서 국가신약개발사업 과제로 선정됐다. 이에따라 SK바이오팜은 SKL2796의 미국 내 임상 1상 연구 및 비임상 연구를 2년간 지원 받을 수 있게 됐다.
이 시각 인기 뉴스
SKL27969는 PRMT5(Protein Arginine Methyltransferase 5)를 선택적으로 억제하는 차세대 항암신약이다. PRMT5는 암세포의 증식 및 성장에 관여하는 단백질의 일종으로, 과발현 시 발암 및 치료 저항에 영향을 미치는 매커니즘이 확인되면서 전세계적으로 주목받고 있다. SK바이오팜은 SKL27969를 뇌종양 및 비소세포폐암, 삼중음성유방암 등 뇌전이암 치료제로 개발한다는 계획이다.
SKL27969의 미국 임상 1상은 18세 이상 성인 96명을 대상으로 16개 의료기관에서 진행한다. 안전성, 내약성, 약동학 등을 평가해 최대 내약용량 및 2상 투여용량을 확인한 후 교모세포종, 비소세포폐암, 삼중음성유방암 등 환자에 대한 예비 항암효과를 평가한다.
카리스바메이트와 SKL27969는 SK바이오팜이 세노바메이트의 뒤를 이을 신약으로 개발역량을 쏟는 파이프라인(신약후보물질)이다. 뇌전증 신약 세노바메이트는 올해 미국 매출이 이미 1000억원을 돌파해 글로벌 블록버스터 문턱에 섰다. 하지만 SK바이오팜으로서는 세노바메이트를 제외하면 뚜렷한 수익원이 없는 상태다. 시간이 지나면 특허 만료 및 또 다른 신약 등장에 따라 시장 장악력이 약해지는 신약 숙명을 감안하면 세노바메이트의 뒤를 잇는 블록버스터 신약이 나와야 한다. 회사가 카리스바메이트와 SKL27969에 힘을 쏟는 이유다.
한 업계 관계자는 "SKL27969가 겨눈 뇌종양, 비소세포폐암, 삼중음성유방암 치료제 시장 규모는 12조원에 육박하지만 항암치료제 성격상 개발에 긴 시간이 필요할 것"이라며 "상대적으로 개발 속도가 빠른 카리스바메이트는 이르면 2025년 출시가 가능할 것으로 보인다"고 말했다.
