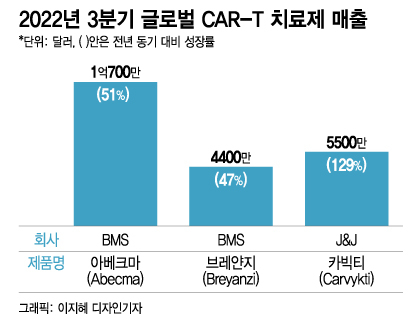
30일 업계에 따르면 올해 3분기에도 CAR-T 세포 치료제의 글로벌 매출이 크게 성장했다. 미국 소재 빅파마 BMS는 25일(현지 시각) 실적 발표에서 자사의 CAR-T 치료제 '아베크마' 3분기 매출이 1억700만 달러를 기록했다고 밝혔다. 전년 동기 대비 51% 증가했다. 또 다른 CAR-T 치료제 '브레얀지'도 4400만 달러 매출을 기록하며 전년 동기 대비 47% 성장했다.
CAR-T는 개인의 면역세포를 추출·가공해 다시 환자에 투여하는 치료제다. 림프종과 백혈병 등 혈액암에서 높은 약물 반응성을 자랑한다. 효과가 좋아 의료 현장에서는 "죽을 환자 100명 중 30명을 살릴 수 있다"는 평가가 나온다.

앱클론은 올해 5월부터 서울아산병원을 중심으로 임상을 진행했는데 의료기관을 아주대병원, 울산대병원, 동아대병원 세 곳으로 확장한 것이다. 앱클론 관계자는 "전국 혈액암 환자분들이 서울뿐 아니라 각 지역 병원에서도 최첨단 의료 서비스를 받으실 수 있기를 기대한다"며 "CAR-T 치료제 공급 체인을 확보함으로써 임상 속도를 한 층 더 끌어올리는 데 주력하고 있다"고 말했다.
앞서 이종서 앱클론 대표이사는 주주들에게 보내는 메시지에서 "AT101 최소량을 투여받은 상당수 혈액암 환자에게서 완전 관해의 결과가 얻어지고 있다"며 "임상 1상 완료 시점은 내년 상반기로 예상한다"고 밝혔다.
이 시각 인기 뉴스
큐로셀은 지난해 2월부터 식품의약품안전처로부터 'CRC01' 임상 1/2상을 허가받아 진행 중이다. 먼저 재발·불응성 거대 B세포 림프종 성인 환자 치료제로 임상을 진행했으며 곧 B세포 성인 백혈병 환자를 대상으로도 임상을 시작할 예정이다.
올해 6월 유럽혈액학회에서 회사가 발표한 임상 중간 데이터에 따르면 CRC01를 투여받은 B세포 림프종 환자 11명 중 9명(82%)이 완전 관해에 도달했다.
긍정적인 임상 결과는 해외 파트너십 체결로 이어질 수 있다. 존슨앤드존슨의 카빅티는 원래 중국의 레전드바이오텍이 개발하던 치료제였다. 2017년 카빅티의 긍정적 임상 결과가 발표되자 존슨앤드존슨이 3억5000만 달러를 지불하고 레전드바이오텍으로부터 라이선스를 가져왔다.
업계 관계자는 "지금까지 나온 모든 혈액암 치료제에서 가장 효과가 좋은 게 CAR-T"라며 "아직 부작용과 생산 등 이슈로 개발에 어려움이 있지만 성공 시 상업적으로 크게 성공할 수 있다"고 설명했다.
