
써나젠테라퓨틱스는 바이오니아가 개발한 신약 플랫폼과 이를 기반으로 개발한 SRN-001 등 신약후보물질에 대해 특허 전용실시권을 갖고 있다. 양사는 국내와 미국, 독일, 호주, 중국, 일본 등 주요국에 신약 구조체 원천특허와 신약후보물질 특허 등 190여 건의 지식재산권을 보유, 난치병 신약 개발을 위한 독점적이고 강력한 지위를 확보하고 있다.
SRN-001은 폐·신장 조직 등의 섬유화에 관여하는 성장인자인 AREG(amphiregulin)를 합성하는 mRNA를 분해, 해당 성장인자가 만들어지는 것을 억제한다. 임상시험은 내년 진입이 예정돼 있다.
박준영 써나젠테라퓨틱스 최고전략책임자(CSO)는 "전임상 연구에서 특발성 폐섬유증, 만성 신장질환(CKD)에 대한 효능과 안전성을 확인했다"고 말했다.
이 시각 인기 뉴스
 /자료=바이오니아
/자료=바이오니아SRN-001은 뛰어난 항섬유화·항염증 효과와 생체 내 안정성·안전성을 보였다. 특히 미국 식품의약국(FDA) 허가를 받아 시판 중인 짧은 간섭(small interfering) RNA인 siRNA 기반 치료제들도 극복하지 못한 선천면역반응 유발 부작용이 나타나지 않았다. 생명에 직접적 영향을 미치는 심혈관계·호흡기계·중추신경계 기능에 악영향을 미치지 않는 등 약리학적 안전성도 확인됐다. 해당 전임상 연구 결과는 국제학술지 JBC(The Journal of Biological Chemitry), 사이언티픽 리포트(Scientific Reports) 등에 눈문으로 발표됐다.
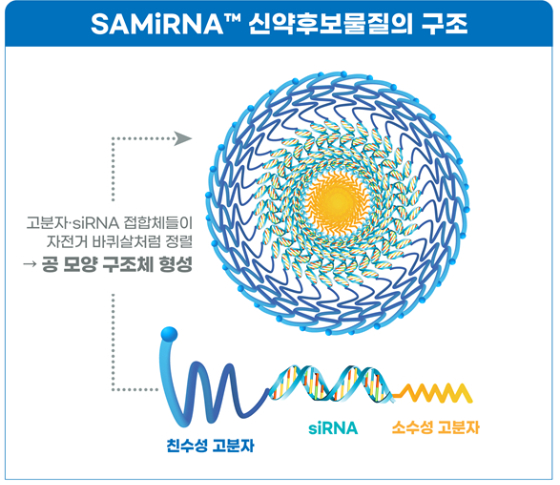
siRNA는 질병 단백질 등 표적 단백질을 만드는 mRNA를 분해하는 20 염기쌍(bp) 안팎의 이중 가닥 RNA로 질병을 근본적으로 치료할 수 있는 잠재력을 가졌다. 하지만 혈액·세포에서 쉽게 분해되고 표적 장기·조직으로의 전달 효율이 크게 떨어진다. 바이오니아는 이런 문제점을 해결하기 위해 siRNA 양끝에 각각 친수성·소수성 고분자를 붙인 단일분자들이 스스로 자전거 바퀴살처럼 정렬되면서 공 모양으로 뭉쳐지는 신약 구조체인 SAMiRNA™(Self-Assembled micelle inhibitory RNA)를 발명했다.
이를 통해 친수성 고분자들이 약물 바깥쪽을 감싸고 크기가 나노 수준(지름 약 80~90㎚)이라 siRNA가 혈액·세포 내 각종 효소에 의해 쉽게 분해되지 않고 선천면역을 자극하지 않는다. 표적 조직·세포로의 전달과 세포막 통과, 독성 감소에 이상적이다. 표적 단백질에 따라 이를 만드는 mRNA 분해 효율이 높은 siRNA로 바꿔주면 신약후보물질을 신속하게 개발할 수 있다는 설명이다.
