
28일 바이오업계에 따르면 FDA는 최근 블루버드바이오의 진테글로를 수혈 의존성 베타 지중해빈혈 치료제로 승인했다. 수혈 의존성 베타 지중해빈혈은 베타 글로빈 유전자 돌연변이로 헤모글로빈이 줄거나 없어지는 희귀질환이다. 평생 수혈을 통해 헤모글로빈 수치를 유지해야 하므로 환자 삶의 질 저하가 크다. 미국에서 해당 질환을 앓는 환자는 약 1500명으로 추정된다.
FDA의 진테글로 승인은 제약·바이오 업계에서 의미가 크다. 우선 FDA가 수혈 의존성 베타 지중해빈혈 치료제를 승인한 건 이번이 처음이다. 또한 희귀 안질환 치료제 '럭스터나'와 척수성 근위축증 치료제 '졸겐스마'에 이어 세 번째로 승인받은 유전자 치료제이기도 하다.
비싼 약값은 진테글로가 극복해야 할 단점이다. 시장 진출에 걸림돌이 될 수 있기 때문이다. 진테글로는 지난 2019년 유럽에서 허가받았지만 이후 시장에서 철수했다. 비싼 가격으로 가격 합의에 실패한 게 원인이었다.
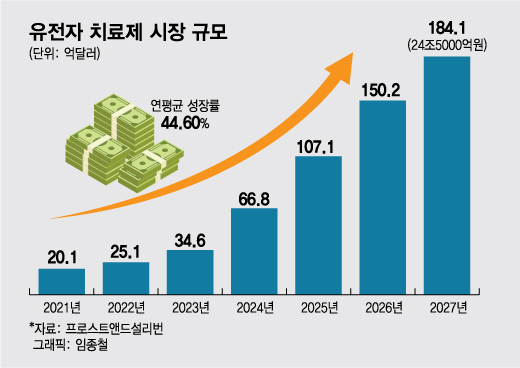
박봉현 한국바이오협회 책임 연구원은 "유전자 치료제 시장은 연평균 44.6% 증가하고, 오는 2027년 184억 달러(약 24.5조원)로 성장해 전체 세포·유전자 치료제 시장 규모인 417억 달러에서 44%를 차지할 것으로 전망된다"고 밝혔다.
이 시각 인기 뉴스
'렌티바이러스 벡터'를 이용한 유전자 치료제도 주목받을 것으로 보인다. 진테글로는 FDA가 승인한 최초의 렌티바이러스 벡터 치료제다. 바이러스 벡터 기술은 변형한 바이러스를 약물 전달 수단으로 이용하는 것이다. 바이러스에 특정 유전자를 싣고, 이 바이러스를 환자에 투입해 세포까지 도달하게 한다.
바이러스 벡터 유전자 치료제는 대부분 AAV(Adeno-associated Virus)로 개발된다. 렌티바이러스 벡터 기전의 비중은 10%밖에 되지 않는다. 이번 진테글로 등장으로 렌티바이러스 벡터 기전에 대한 관심도 높아질 전망이다. 국내 기업에서는 차바이오텍 (16,510원 ▼390 -2.31%)이 관련돼 있다. 차바이오텍 자회사 마티카 바이오테크놀로지는 최근 미국에서 CDMO(위탁 개발·생산) 시설을 준공했는데 이곳에서 렌티바이러스 벡터 등 유전자 치료제 핵심 원료를 생산할 계획이다.
