24일 업계에 따르면 최근 국제학술지 '사이언스(Science)'는 2006년 '네이처'에 발표된 미네소타대학의 논문이 조작됐을 수도 있다는 과학계 의견을 보도했다. 이 논문은 쥐를 이용한 동물실험에서 알츠하이머를 유발하는 단백질인 '아밀로이드베타*56'를 발견했다는 내용을 담고 있다.
알츠하이머는 치매 유발 원인의 50~70%를 차지하는 퇴행성 뇌 질환이다. 논란이 된 논문은 지난 16년간 약 2300여 건 인용되면서 아밀로이드베타 단백질 침착이 알츠하이머를 유발한다는 가설의 근거가 됐다. 제거되지 못한 아밀로이드베타 단백질이 플라크(plaque) 형태로 쌓이면 산화적 스트레스를 유발, 뇌 신경 세포를 손상한다는 원리다.
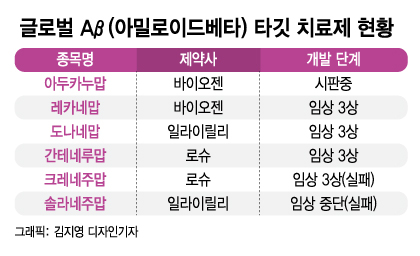
임상시험 등록 사이트 클리니컬트라이얼즈(Clinicaltrials.gov)에 따르면 2021년 초반 기준, 알츠하이머 관련 126개 후보물질에서 총 152건의 임상이 진행 중이다. 28개가 임상 3상까지 올라왔으며 이 중 5개가 아밀로이드베타 단백질을 표적하는 기전이다.
2006년 논문의 조작이 사실이라면 아밀로이드베타 가설에 근거해 시간과 돈을 투자했던 제약업계에 큰 피해가 예상된다. 실제로 최근 글로벌 제약사의 치매 치료제 개발 성적은 좋지 않았다.
이 시각 인기 뉴스
아밀로이드베타 플라크 제거 기전으로 처음 승인받은 치매 치료제 '아두카누맙'은 허가 이후에도 유효성 논란을 일으켰다. 개발사 바이오젠이 약가를 50%까지 낮추는 등 노력했지만 끝내 아두카누맙은 미국 보험 적용에서 제외됐다.
일라이릴리의 '솔라네주맙'은 지난 2016년 임상 3상에 실패해 일찌감치 개발이 중단됐다. 최근에는 로슈가 자사의 알츠하이머 치료제 후보물질 '크레네주맙'이 임상 3상 1차 평가지수를 충족하지 못했다고 발표하기도 했다.
바이오젠의 '레카네맙', 일라이릴리의 '도나네맙', 로슈의 '간테네루맙'은 올해 하반기 임상 3상 결과를 발표할 것으로 예상된다. 모두 아밀로이드베타 기전의 약으로 향후 이들 치료제의 성공 여부가 논문 조작 의혹 진실 공방에 결정적 역할을 할 것으로 보인다.
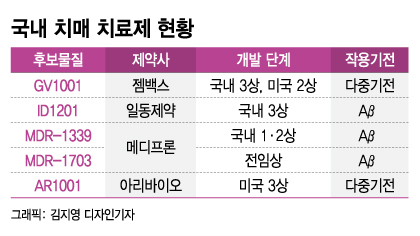
아리바이오의 후보물질 'AR1001'은 아밀로이드베타뿐만 아니라 타우(Tau) 단백질을 표적해 제거하고, 신경세포 시냅스 형성을 늘리는 등 여러 기전으로 치매를 공략한다. 젬백스앤카엘의 'GV1001'도 다중기전 치료제로 알려졌다. 메디프론의 'MDR-1339'와 'MDR-1703'은 아밀로이드베타 독소를 표적하지만 회사는 이 외에도 타우 독소를 공략하는 후보물질을 개발하는 등 파이프라인을 다양화했다.
아밀로이드베타 가설이 완전히 사장된 건 아니라는 신중론도 존재한다. 이번에 논란이 된 2006년도 논문은 '아밀로이드베타*56'라는 단백질의 존재를 다룬다. 하지만 알츠하이머 임상에서 주로 연구하거나 타깃하는 단백질 그룹은 '아밀로이드베타 1-40 및 1-42'다.
업계 관계자는 "이번 논문 사건에서 문제가 된 단백질 그룹이 '*56'이므로 아밀로이드베타 가설이나 지금까지 나온 알츠하이머 연구를 전부 부정하는 건 과장일 수 있다"고 설명했다.
