희귀질환 분야는 천문학적 개발 비용에 불확실성 리스크도 있지만 환자수가 적다는 '틈새시장' 특성 덕분에 선점 효과도 크다. 중증근무력증 치료제 시장은 존슨앤드존슨(J&J)과 아스트라제네카 등 글로벌 빅파마들이 뛰어들면서 최근 각광받는다. 한올바이오파마의 HL161은 경쟁사 제품 대비 더 편리한 투여 방법을 앞세워 시장 진입을 노린다.
현재 중국 파트너사인 하버바이오메드를 통해 임상 3상을 진행 중이다. 미국에서는 이뮤노반트가 동일 적응증으로 임상 3상을 준비하고 있다. 빠르면 상반기 임상을 시작할 것으로 보인다. 또한 이뮤노반트는 하반기에도 일본 임상 3상 진입을 목표하고 있다. HL161 상용화가 성공하면 한올바이오파마는 국내 바이오기업 중에서는 처음으로 중증근무력증 치료제를 개발하게 된다.
중증근무력증은 자가면역질환의 하나로 초기 증상은 눈꺼풀 처짐과 안구 운동 장애다. 진행이 계속되면 전신의 근력이 약화돼 호흡이 어려워진다. 미국 환자 수는 약 6만6000명, 유럽은 10만4000명으로 추정된다.
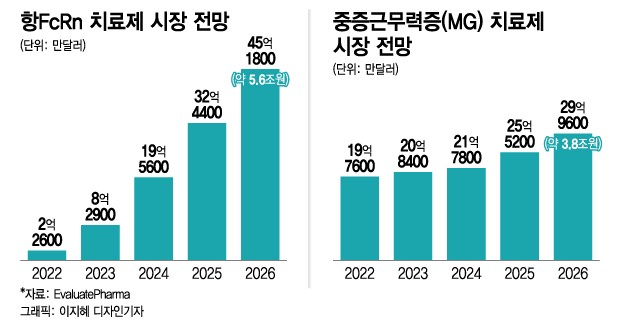
글로벌 시장조사 기관 'Evaluate Pharma'에 따르면 중증근무력증 치료제 시장은 오는 2026년 29억9600만 달러(약 3.8조원) 규모를 형성할 것으로 보인다. HL161의 기전인 항FcRn 치료제는 같은 기간 45억1800만 달러(약 5.6조원) 시장 규모가 전망된다. 2022년 시장 규모가 2억2600만 달러(약 2800억원)임을 감안하면 4년 새 20배나 성장하는 것이다.
이 시각 인기 뉴스
기존 중증근무력증 치료제는 의료진이 긴 시간에 걸쳐 투약하는 IV 제형으로 치료를 위해 환자가 병원을 꼭 방문해야 한다는 불편함이 있었다. 이에 HL161은 처음부터 자가 투여가 가능한 SC 제형으로 개발됐다. SC 제형은 IV 제형보다 약가가 높지만 환자의 병원 방문 비용 등이 없어 결과적으로 더 저렴할 것으로 전망된다.
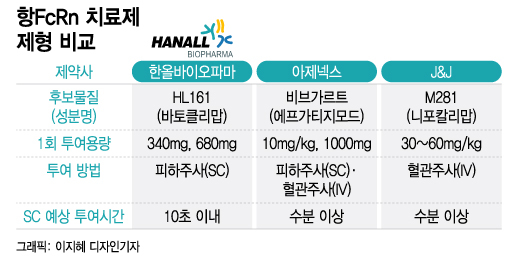
HL161의 SC 제형은 경쟁 제품 대비 적은 용량으로 인한 짧은 투약 시간이 강점이다. HL161의 SC 1회 투여 용량은 340mg와 고용량 680mg으로 나뉘며 투약 시 10초 이내가 걸릴 것으로 보인다. 반면 경쟁사 아제넥스의 비브가르트는 1회 투여량이 1000mg으로 피하 주사 시에도 수분의 시간이 걸릴 것으로 예상된다.
경쟁사의 SC 제형 개발 현황을 보면 한올바이오파마의 HL161은 뒤처지지 않는다. 아제넥스 비브가르트의 SC 제형은 빨라도 내년 하반기에나 출시될 것으로 예상된다. 또 다른 경쟁사 J&J의 M281(성분명: 니포칼리맙)도 SC 제형을 개발하고 있지만 자세한 내용은 공개되지 않았다.
김병조 고려대 안암병원 신경과 교수는 "중증근무력증 환자 중 증상이 심한 경우에는 사지 근력 약화와 호흡 부전까지 발생하여 생명에 위협을 받을 수도 있다"며 "아직 질환 기전에 맞게 개발된 효과적인 치료제는 극히 제한적이어서 부작용이 많은 스테로이드와 같은 범용성 면역 억제제를 사용하고 있는 상황"이라고 설명했다.
김 교수는 "최근 항FcRn 계열 신약이 FDA에서 허가를 받으면서 중증근무력증 영역에서 주목을 받고 있다"며 "한올바이오파마에서 개발하고 있는 항FcRn도 빠르게 환자들에게 사용할 수 있기를 기대한다"고 말했다.
