큐리언트 두번째 항암제 'Q901', 미국FDA 임상 1/2상 승인
머니투데이 고석용 기자
2022.02.08 16:39
큐리언트 (4,370원 ▲120 +2.82%)가 8일 미국 식품의약국(FDA)으로부터 항암치료제 'Q901'의 임상 1/2상 시험을 승인받았다고 밝혔다.
Q901은 미국에서 임상 단계에 진입하는 큐리언트의 2번째 항암 신약이다. 세포 주기 조절 인자들 중 핵심이 되는 CDK7을 저해해 세포 분열 주기에 문제가 생긴 암세포를 사멸시키는 것이 특징이다. 큐리언트 측은 "Q901이 경쟁약물 대비 선택성이 높아 CDK7 저해제로서 해외 학회 등에서 많은 관심을 받았다"고 강조했다.
Q901 임상 1/2상 시험은 약 70명의 진행형 고형암 환자를 대상으로 미국의 주요 병원에서 진행될 예정이다. 용량에 따른 안전성 검증, 유효 용량 확인·항암 효능을 확인하는 것이 목표다.
아울러 큐리언트는 오는 4월 미국 뉴올리언스에서 개최되는 미국암학회(AACR)에서 Q901의 다양한 암종에서의 추가 효능 데이터를 발표할 예정이다
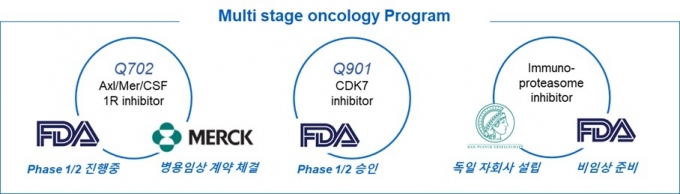
큐리언트 관계자는 "현재 당사에서 개발 중인 항암제 프로그램 2개(Q702, Q901)가 모두 임상에 진입했다"며 "독일 자회사 QLi5에서 개발 중인 면역프로테아좀 저해 기전의 항암제 개발도 순조롭게 진행되고 있다"고 말했다.
그러면서 "복수 기전의 다양한 항암 프로그램들로 안정적인 포트폴리오가 구축되고 있는 만큼 2022년은 큐리언트가 항암신약 전문 바이오텍으로 거듭나는 한 해가 되겠다"고 말했다.
<저작권자 @머니투데이, 무단전재 및 재배포 금지>