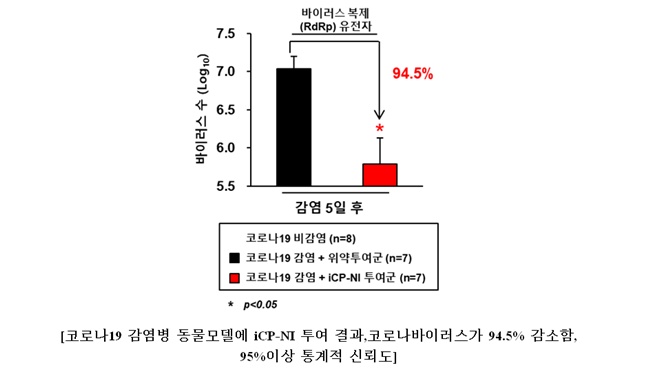
회사 측에 따르면 바이러스 수는 최대 94.5%까지 급감했고, 면역폭풍을 일으켜 위중증 및 사망에 이르게 할수있는 강력한 염증성 싸이토카인들인 인터루킨 (IL)-17은 -68%, 티엔에프-알파 (TNF-α)는 -69% 그리고인터루킨 (IL)-6는 -45% 를 감소시킬 뿐만 아니라, 직접적인 병변부위인 폐 조직을 보호해 영구적 조직손상을 억제하고, 대표적인 임상증상인 몸무게의 급격한 감소까지 회복시키는 등, 평가를 진행한 모든 항목에서 뛰어난 코로나19 치료 효능이 나타났다.
셀리버리는 지난 2020년 초 부터약물재창출이 아닌 바이러스 감염병을 대비한 면역치료신약으로써 iCP-NI를 개발해 왔다.
현재 셀리버리는 iCP-NI 관련해 현재 유럽과 미국에서 임상단계(유럽:임상신청 완료, 미국: 임상신청 단계)를 진행하고 있다.
셀리버리 측은 "임상1상은 사람에게서 안전성을 평가하므로 매우 빨리 진행, 종료될 것이고, 임상2상에서 실제 코로나19 감염병에 대한 치료효능을 평가하게 되는데, 이러한 동물모델의 치료효능 결과가 명확하면, 임상2상 신청 후 평가기간을 대폭 줄일 수 있을 뿐만 아니라, 실제 임상시험 중 용량결정시험 및 투여유효용량을 결정하는데 소요되는 기간을 상당히 단축시킬 근거로 작용하게 돼 코로나19 감염자 대상 임상시험 조기종료에 큰 보탬이 될 것이 분명하다"고고 설명했다.
이 시각 인기 뉴스
이어 "다른 임상물질 및 기존 치료제(예, 항바이러스제 렘데시비르 등)대비 상당히 우수한 결과 도출을 국가공인시험기관에서 증명해 준 것이므로, 이 결과를 한국 식품의약품안전처(KFDA)와 공유해 어떻게 하면 좀더 빨리 코로나19 감염병 치료제로써 임상시험을 완료하고 한국을 포함한 세계 시장에 감염병 치료신약으로 내 놓을 수 있을지 심도 깊게 의논해 현명히 추진하겠다"고 앞으로의 계획을 설명했다.
정희영 머니투데이방송 MTN 기자
