14일 관련 업계에 따르면 식품의약품안전처(식약처)는 콜린알포 제제의 유효성 재평가를 위한 임상시험계획서를 승인했다. 종근당 (101,800원 ▼1,300 -1.26%), 대웅바이오 등 57개 제약사의 133개 품목이 이에 해당한다.
이번 재평가 임상도 콜린알포 제제의 치료 효과를 따져보기 위해 진행된다. 다만, 식약처는 기존에 인정했던 콜린알포의 효능 3개 중 '뇌혈관 결손에 의한 2차 증상 및 변성 또는 퇴행성 뇌기질성 정신증후군' 1개만 인정했다. 감정 및 행동변화, 노인성 가성 우울증 등 기존에 콜린알포 처방이 가능했던 증상은 인정하지 않았다. 따라서 임상을 승인받은 57개 제약사는 치매의 초기증상으로 여겨지는 기억력 저하와 착란, 의욕 및 자발성 저하로 인한 방향감각 장애, 집중력 감소 등 증상에 대해서 효능과 효과를 확인해야 한다.
당국이 콜린알포의 효능 입증에 대해 단호한 자세를 취하고 있는 상황에서 제약사들은 바짝 긴장하는 모습이다.
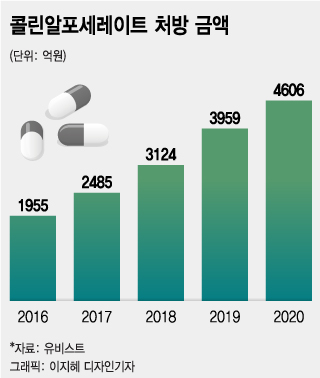
콜린알포는 제약사 입장에서 포기하기 어려운 품목이다. 노인성 질환에 대한 뇌기능 개선제라, 노인층을 타깃으로 삼는 의약품이다. 국내에서 정식 허가받은 치매 치료제가 없는 데다가 노령층 환자들의 수요가 늘면서 시장 규모가 매년 대폭 성장하고 있다. 의약품 조사기관 유비스트에 따르면 2016년 1955억원 규모였던 콜린알포 처방 규모는 지난해 4606억원으로 5년 새 2배 이상 늘었다.
이 시각 인기 뉴스
이 뿐 아니라, 재평가 임상시험에 실패할 경우 임상을 진행하는 동안 처방된 금액에 대해 환수가 이뤄질 수 있다는 점에서도 긴장을 놓칠 수 없다. 보건복지부는 국민건강보험공단에 콜린알포 제제 230개 품목에 대해 요양급여계약을 명령했다. 제약사가 재평가 임상에 실패하면 임상계획서를 제출한 날부터 품목허가가 취소되는 날까지 처방액 전액을 반환해야 한다는 것이 주 내용이다. 건보공단과 제약사들은 재평가 임상에서 실패할 경우 제약사가 부담해야 하는 환수율에 대해 합의하고 있다.
제약사들은 복지부의 환수협상 명령에 소송으로 대응하고 있으나, 순탄치 않은 상황이다. 대웅바이오와 종근당을 주축으로 각각 28개사가 참여한 2건의 복지부 환수협상 명령 불복 행정소송과 집행정지 관련 소송 모두 1·2심에서 기각됐다.
업계 관계자는 "콜린알포는 지속적으로 성장세를 보이는 만큼 놓치기 어려운 시장이 될 수밖에 없다"면서 "적응증이 3개에서 1개로 줄어 이전보다 제한이 생긴 만큼 시장에 남기 위해서라도 성공률을 높이기 위해 임상에 매진할 것으로 보인다"고 말했다.
