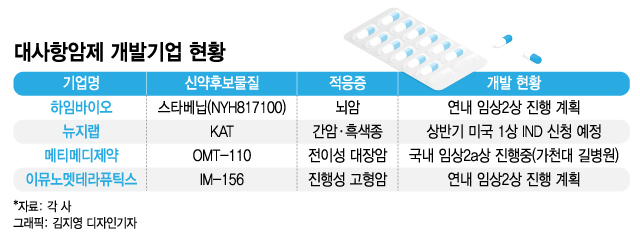
13일 관련업계에 따르면 하임바이오는 4세대 대사항암제 '스타베닙'(NYH817100)의 임상 1상 결과를 발표하고 연내 국내 임상 2상에 착수할 계획이다.
'스타베닙'은 기존에 존재하던 물질로 약을 개발하는 약물 재창출 방식의 신약이다. 목화씨 기름에서 유래한 물질인 '고시폴'(NYH817G)과 당뇨약으로 쓰이는 '펜포르민'(NYH100P)을 을 병용해 암세포의 에너지 대사를 차단하는 치료제다.
뉴지랩은 2019년 5월 미국의 항암 신약 물질 개발 전문기업인 '고디스커버리'(KoDiscovery LLC)에서 대사항암제 기술 KAT를 이전받았다.
KAT는 암세포에서 과발현하는 헥소키나아제2와 결합하는 치료제다. 헥소키나아제2는 세포자살을 막아 암세포가 성장할 수 있도록 돕는다. 암세포에 침투시킨 물질이 헥소키나아제와 결합할 경우 암세포의 에너지 생산을 중단시켜 굶어 죽게 만든다.
이 시각 인기 뉴스
메티메디제약은 가천대 길병원에서 전이성 대장암 적응증으로 'OMT-110'의 임상 2a상을 진행중이다. 'OMT-110'은 암세포가 정상세포와 다르게 세포의 주 에너지원인 포도당을 비정상적으로 많이 소모하는데 착안한 항암제다. 암 세포의 대사체계를 일반 세포와 동일하게 전환해 사멸을 유도한다. 'OMT-110'도 약물재창출 방식의 신약후보물질이다.
현재 대사항암제로서 규제기관을 통과한 약품은 미국 아지오스 사의 급성 골수성 백혈병 치료제인 아이드하이파가 유일하다. 미국 FDA(식품의약국)는 2017년 8월 특정 유전자(IDH2) 돌연변이가 확인된 재발불응성 급성골수성백혈병으로 진단받은 성인 환자에 한해 치료제로 승인한 바 있다.
대사항암제의 안전성과 효과성을 두고선 아직 의료계의 의견이 분분하다.
국내에서 개발중인 대사항암제는 대체로 독성평가 단계인 임상 1상 단계는 무난히 넘어서고 있다. 임상 1상에선 주로 약물의 체내 흡수, 분포, 대사, 배설 등의 약동학적 효과와 부작용 여부를 확인하는 실험이 진행된다.
바이오업계 관계자는 "대사항암제는 기존 항암제와는 달리 독성이 매우 낮다는 장점이 확실하다"며 "약효나 적정용량을 평가하는 임상 2상 이후가 대사항암제 원천 기술을 확보하는 기로가 될 것"이라고 말했다.
반면 일부에선 암세포의 대사를 조절하는 과정에서 정상세포의 대사과정에 부정적인 영향을 줄 수밖에 없다는 지적도 나온다.
증권업계 관계자는 "아직 글로벌 제약사들은 여전히 3세대 항암제와 자가면역질환 치료제에 관심이 높은 편"이라며 "암세포만 특정해 대사활동을 막는다는 대사항암제가 주류가 되기 위해선 아직 임상 등의 연구결과가 많이 필요한 상황"이라고 말했다.
