제넥신, 백신 임상 첫 투여
21일 관련업계에 따르면 제넥신 (7,280원 ▼70 -0.95%)은 코로나19 DNA 백신 'GX-19' 임상 1·2a상 첫 대상자 투여를 마쳤다. 회사는 건강한 성인 자원자를 대상으로 임상을 진행해 안전성, 면역원성 등을 확인할 예정이다.
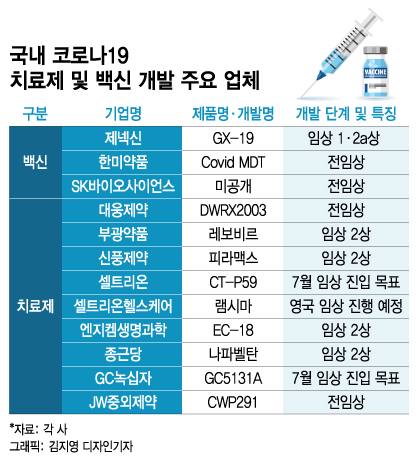
이로써 국내에서 코로나19 백신·치료제 임상 승인을 받은 업체는 제넥신, 종근당, 부광약품 (6,150원 0.00%), 신풍제약 (13,640원 ▲280 +2.10%), 엔지켐생명과학 (1,880원 ▲13 +0.70%) 등 5곳으로 늘었다. 제넥신을 제외한 나머지 업체들은 모두 임상 2상 단계다.
업계에서는 식약처가 코로나19 치료제에도 조건부 허가 제도를 적용하면 임상 2상 후 바로 치료제가 나올 수 있을 것으로 본다.
GC녹십자·셀트리온, 7월 임상진입 목표
앞으로 코로나19 백신·치료제 임상은 증가할 것으로 예상된다. 크리스탈 (3,130원 ▲30 +0.97%)지노믹스는 지난달 말 췌장염 치료제 '카모스타트'의 코로나19 임상 2상 시험을 식약처에 신청했다.
이 시각 인기 뉴스
GC녹십자 (111,900원 ▲800 +0.72%)는 다음 달 코로나19 혈장치료제 'GC5131A' 임상을 시작하고, 연내 치료제를 출시할 계획이다. 셀트리온 (176,600원 ▼800 -0.45%)도 다음 달 코로나19 항체치료제 'CT-P59' 임상 진입을 목표로 하고 있다. SK바이오사이언스는 이르면 오는 9월 코로나19 백신 임상을 시작할 계획이다.
해외에서 코로나19 치료제 개발을 진행하는 국내 업체들도 있다. 셀트리온헬스케어 (75,900원 ▼4,500 -5.60%)는 영국 옥스퍼드대학교와 자가면역치료용 바이오시밀러(바이오의약품 복제약) '램시마'의 코로나19 치료 효과를 확인하는 임상을 시작할 예정이다. 일양약품 (13,710원 ▲30 +0.22%)은 지난달 러시아 정부로부터 백혈병 치료제 '슈펙트'를 코로나19 치료제로 개발하는 임상 3상을 승인받았다.
대형 제약사도 코로나 치료제 개발 도전
최근에는 대웅제약 (112,700원 ▲2,200 +1.99%), 한미사이언스 (33,500원 ▲200 +0.60%), JW중외제약 (30,400원 ▲600 +2.01%) 등 대형 제약사들이 코로나19 백신·치료제 개발에 도전장을 던졌다.
대웅제약은 대웅테라퓨틱스, 한국파스퇴르연구소와 함께 구충제인 '니클로사마이드' 성분 치료제 'DWRX2003'을 코로나19 치료제로 개발 중이다. 회사는 오는 7월 식약처에 임상을 신청할 계획이다.
JW중외제약은 항암제로 개발 중인 'CWP291'을 코로나19 치료용 조성물로 특허 출원했다. 회사는 CWP291이 바이러스가 세포에 진입하고 복제하는 것을 억제할 것으로 보고있다.
한미사이언스는 바이오 벤처 바이오앱과 함께 코로나19 백신을 개발할 계획이다. 또 이와 별도로 주사제를 먹는 약(경구용)으로 바꾸는 기술인 '오라스커버리'를 적용한 경구용 코로나19 백신도 개발 중이다.
