식품의약품안전청은 의약품 수출을 위해서 국내 제약사가 수입국의 규제기관이나 수입업체로부터 받은 GMP(우수의약품 제조·관리 기준)실사가 2005년 25건에서 2010년 63건으로 증가했다고 9일 밝혔다.
식약청은 2008년 국내 GMP의 기준을 선진국 수준으로 강화한 새 GMP제도를 도입했다. 새 GMP 제도는 허가 후 제형별 평가에서 품목별 사전 평가로 전환하는 것이 핵심이었다.
식약청은 수출 희망업체에 대해서는 식약청 조사관이 사전 모의실사를 진행해 해외실사를 대비할 수 있도록 하는 등 적극 지원에 나섰다. 식약청은 지금까지 20건의 모의실사를 해줬다.
이에 따라 국내 제약사의 의약품 수출실적도 증가하고 있다. 식약청에 따르면 국내 의약품 수출실적은 2007년 10억2000만달러에서 2008년 11억4000만달러, 2010년 17억1000만달러로 증가했다.
이 시각 인기 뉴스
식약청은 앞으로도 국내 제약업체들이 GMP 수준을 더욱 향상시켜 국제 경쟁력을 높여 나갈 수 있도록 하기 위해 △제약-IT 융합 생산·품질관리시스템 보급 △해외 수출 희망업체 사전 모의실사 프로그램 운영 △현장 중심 밸리데이션 실무교육 실시 등을 실시할 예정이다.
또 수출국과의 상호 실사면제 등 국가간 상호인증(MRA)체결을 추진하는 등 국제 경쟁력을 높여 나갈 수 있도록 지원을 강화할 계획이다.
[국내제약업체 대상 국외 규제기관 등 실사 횟수]
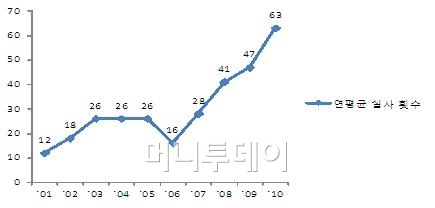 ↑ 자료:한국제약협회
↑ 자료:한국제약협회