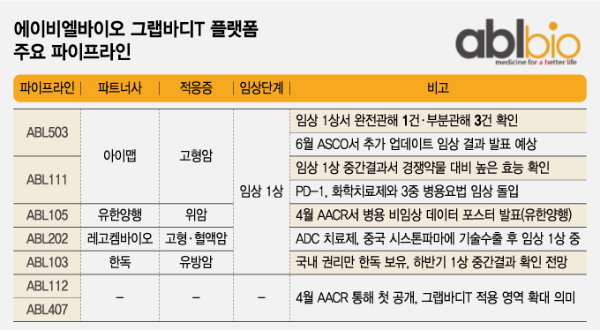
21일 에이비엘바이오에 따르면 이 회사는 올해 이중항암항체 플랫폼 그랩바디-T를 기반으로 한 다수 신약 후보물질 임상 결과를 내놓는다. 그동안 개발 초기에 머물렀던 신약 후보들이 속속 본개발에 진입하게 되는 만큼, 후속 기술수출 주자로의 가능성도 한층 커질 전망이다.
에이비엘바이오의 이중항체 플랫폼은 크게 세가지로 나뉜다. BBB 셔틀 기반으로 CNS 질환을 공략하기 위한 그랩바디-B와 4-1BB 기반 이중항체를 타깃으로 하는 종양(항암) 타깃 그랩바디-T, 면역조절제 기반 이중항체를 활용한 면역질환 치료용 '그랩바디-I' 등이다.
하지만 올해 에이비엘바이오의 핵심 동력은 그랩바디-T 기반 항암신약 분야다. 지난해 초기 임상 결과를 통해 계열 내 최고신약 가능성을 내비친 파이프라인의 임상 진전을 비롯해 플랫폼 활용 영역을 한층 확장시킨 신규 파이프라인도 첫 공개를 앞두고 있다.
특히 완전관해는 난소암에서, 부분관해는 피부암, 위암 및 두경부암 등에서 확인되며 다양한 암종에서의 효과 기대감을 높인 상태다. 올해 상반기 안에 1상 중간 결과 발표가 예상된다. 경쟁 물질은 덴마크 젠맙의 품목 정도가 꼽히는데 속도는 앞서 있지만(임상 2상) 임상 1/2상 용량 확장에서 100mg 제한적인 투여 용량의 한계를 보였다. 반면, ABL503은 100mg을 초과한 투여에도 독성을 보이지 않아, 역전 발판을 마련한 상태다.
위암 치료제로 개발 중인 ABL111은 지난해 10월 임상 1상 중간결과 발표를 통해 계열내 최고신약(베스트인클래스) 가능성을 높인 상태다. ABL111은 면역세포 활성화를 유도하는 4-1BB와 위암 및 췌장암 핵심 표적 인자로 알려진 클라우딘(Claudin)18.2를 이중 타깃하는 기전이다.
이 시각 인기 뉴스
경쟁 약물로는 클라우딘18.2를 단일 타깃으로 하는 아스텔라스의 '졸베툭시맙'이 꼽힌다. 현재 미국과 유럽에서 허가절차를 진행 중이다. 하지만 ALB111은 임상을 통해 졸베툭시맙 대비 10%포인트 가량 높은 객관적반응률(ORR)을 확인했고, 3등급 이상의 심각한 부작용 발생률은 0%로, 2~12% 수준의 졸베툭시맙을 압도했다.
ALB111의 가치는 병용요법에서 부각될 전망이다. 현재 위암 분야 대표 치료제는 BMS 옵디보로 머크 키트루다가 추격자 위치에 있다. 모두 효능은 좋지만 반응률이 좋지 않아 꾸준히 병용 파트너를 찾고 있는 품목들이다. 하지만 기존 항암화악요법과 병용해도 사망 위험률을 20% 낮추는데 그치고 있다.
이 같은 상황에서 ABL111D은 아이맵을 통해 1분기 면역항암제·항암화학요법과의 3중 병용 임상에 돌입한 상태다. 아직 전략적 이유에서 세부 임상 단계를 공개하진 않았지만 초기 데이터 만으로도 글로벌 제약사들의 눈길을 끌기 충분한 연구라는 평가다.
이밖에 레고켐바이오와 공동 개발해 중국 시스톤으로 기술이전 후 임상 1상을 진행 중인 항체-약물접합체(ADC) 이중항체 신약 'ABL202'도 올 상반기 결과 도출이 예상된다. 유한양행에 넘긴 위암 치료제 'ABL105'는 내달 5일부터 개최되는 미국암학회(AACR)을 통해 병용 비임상 데이터를 발표한다. 특히 올해 AACR에선 그랩바디-T를 적용한 신규 면역항암제 'ABL112'와 'ABL407'의 비임상 데이터가 처음로 공개된다. 한독이 국내 권리를 보유한 유방암 치료제 'ALB103'은 하반기 1상 중간 결과가 확인 가능할 것으로 보인다.
에이비엘바이오 관계자는 "현재 회사가 가장 무게를 두고 있는 ABL503과 3중 병용 임상에 돌입한 ABL111을 필두로 파트너사들이 진행 중인 주요 항암 물질들의 임상 결과 역시 연내 연달아 확인이 가능할 것으로 보인다"며 "처음으로 연구결과를 공개하는 두 파이프라인 역시 기존 종양 항원이 아닌 종양에 밀집한 면역 세포 특이적 항원을 표적하고 있어 그랩바디-T의 적용 영역을 확대했다는 의미가 있다"고 말했다.
