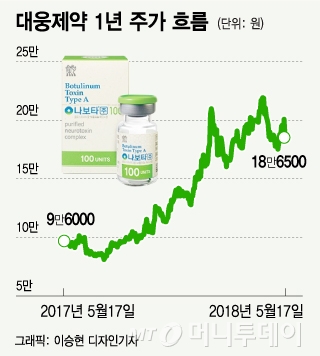
17일 코스피 시장에서 대웅제약 (110,500원 ▼1,100 -0.99%)은 1만4500원(7.21%) 하락한 18만6500원에 마감했다. 올 1월12일 22만7500원으로 사상 최고가를 기록한 뒤 나보타 미국 판매와 관련된 이슈가 터질 때마다 변동성이 커지고 있다.
앞서 2017년 5월 에볼루스는 FDA에 나보타 판매 허가 신청을 냈다. 그 해 11월 FDA는 나보타 제조 공장 실사를 진행했고 올해 1월 지적사항을 담은 문서인 Form483을 발부했다. 당시 FDA의 제조공정 관련 위반사항 지적 사실이 시장에 알려져 대웅제약 주가는 11% 급락했다.
전문가들은 올 하반기로 예상됐던 나보타의 미국 판매 시점이 내년 상반기로 지연될 것으로 관측했다.
서근희 KB증권 연구원은 "늦어도 8월 중 나보타의 미국 판매허가를 예상했으나 이번 발표로 내년 1분기에 승인 날 것으로 판단된다"며 "FDA 자료 보완요구로 인한 허가 지연은 아쉬운 상황이고 재심사 진행 속도에 따라 매수 기회가 생길 것"이라고 분석했다.
이 시각 인기 뉴스
FDA로부터 최종보완요구 공문(CRL)을 받으면 보완 자료를 준비해 재심사를 받아야 한다. 보완할 내용에 따라 1급 심사 대상과 또는 2급 심사 대상으로 분류되며 각각 2개월, 6개월의 시간이 소요된다. 에볼루스는 이번 건이 2급 심사 대상일 것으로 예상된다고 밝혔다. 이에 따라 재심사까지 90일, 허가까지 6개월이 걸려 2019년 봄 미국 발매를 전망했다.
대웅제약의 향후 주가 전망에 대해선 견해가 엇갈렸다. 예상 발매 시점이 올 하반기에서 내년 상반기로 변경되자 목표주가를 하향조정한 애널리스트도 있지만 저가 매수 기회라는 관점도 제기됐다.
구자용 DB금융투자 연구원은 "승인 지연은 어느 정도 예상했지만 승인 시점이 하반기에서 내년으로 밀려난 점에서 신약 가치에 대한 재고가 필요하다"며 "허가 전 주가가 이미 1조원 수준의 신약 가치를 반영하고 있어 당분간 주가 상승은 제한적일 것"이라고 판단했다.
반면 구완성 NH투자증권 연구원은 "안전성, 유효성, 생산 설비 등 주요 이슈가 해결된 상황에서 이번 자료보완 요구는 작은 문제로 보인다"며 "그간 시장의 가장 큰 우려였던 생산설비 문제가 완전히 해소된 것으로 판단돼 이번 자료보완 통지로 인한 주가 하락은 오히려 매수 기회"라고 주장했다.
